Apoptóza (řecká apoptóza - padání listů) je proces programované buněčné smrti, je to zcela přirozený jev, který umožňuje odstranění abnormálních, poškozených a použitých buněk z těla. Stojí za to zjistit, co přesně to je, zda je apoptóza škodlivá, kdy k ní dochází a jaké procesy k ní vedou.
Obsah:
- Zahájení apoptózy
- Průběh apoptózy
- Kontrola apoptózy
- Apoptóza a nemoci
Apoptóza je fyziologický, přirozený proces, který probíhá nepřetržitě v každém zdravém organismu, je nezbytný pro správné fungování organismu. Díky apoptóze má tělo schopnost kontrolovat počet a kvalitu buněk. Tento proces, známý jako programovaná buněčná smrt, vede k eliminaci poškozených, infikovaných nebo nepotřebných buněk a zajišťuje rovnováhu mezi tvorbou nových buněk a destrukcí starých buněk.
Poruchy v průběhu apoptózy mají velmi negativní účinek, existují nemoci, jejichž prevence a léčba je velmi obtížná - rakovina, autoimunitní onemocnění. Snad se nové metody léčby, které umožní proces apoptózy v rakovinných buňkách, stanou efektivní metodou léčby.
Celkový počet buněk v těle je přísně stanoven a konstantní, jakákoli déle trvající změna jejich počtu může mít negativní dopad na naše zdraví, proto se tělo snaží udržovat rovnováhu mezi ničením buněk a tvorbou nových. Proces buněčné smrti může nastat několika způsoby, z nichž nejdůležitější jsou:
- Nekróza (nekróza) - je způsobena vnějšími faktory: chemickými, mechanickými, fyzikálními. Je to patologický, abnormální proces, nad kterým tělo nemá žádnou kontrolu. V jeho průběhu jsou zničeny celé skupiny buněk a důsledkem tohoto poškození je vývoj zánětlivého procesu.
- Apoptóza (programovaná buněčná smrt) je velmi odlišná, proces je zcela normální, fyziologický, jednobuněčný a nezbytný v normálně fungujícím organismu.
- Autofagie - zahrnuje trávení buněk vlastními enzymy.
Navzdory negativním dopadům je apoptóza běžným, běžným jevem, zaměřuje se na dobro celého organismu a umožňuje nahrazení neúčinných, opotřebovaných buněk novými. Odstraněné buňky jsou hlavně ty, které by se mohly stát pro hostitele nebezpečné, např. Rakovinné nebo neoplastické.
Apoptóza tedy pomáhá udržovat homeostázu, tj. Rovnováhu organismu. Proces programované buněčné smrti je velmi složitý jev zahrnující desítky enzymů a proteinů. Doba jejího výskytu také není náhodná, je určena mnoha signálními cestami, které se aktivují v důsledku poškození buněk: jejími organelami nebo genetickým materiálem.
Přečtěte si také: Martwica - co to je? Druhy nekrózy
Zahájení apoptózy
Aktivace apoptózy je spojena s aktivací nebo inhibicí působení určitých proteinů (pro a anti-apoptotických), které jsou v buňce neustále přítomny. Způsob, jakým proces probíhá, závisí na typu a stimulu, který spouští apoptózu. Iniciace je první, počáteční fáze, během níž jsou aktivovány signální dráhy vedoucí k vývoji procesu programované smrti.
Nejdůležitější z nich je takzvaná vnitřní dráha, ve které hrají dominantní roli mitochondrie, a vnější dráhou, jejíž spouštěči jsou signály z vnějšku buňky:
- nedostatek růstových faktorů, hormonů
- zvýšení koncentrace některých cytokinů (molekul produkovaných lymfocyty)
- interakce se sousedními buňkami
- fyzikální faktory
- nedostatek živin.
V případě vnější cesty působí stimuly prostředí na receptory umístěné v buněčné membráně (tzv. Receptory smrti), které spouští kaskádu intracelulárních signálů vedoucích k apoptóze.
V případě vnitřní dráhy hrají klíčovou roli mitochondrie. Po jejich poškození různými faktory se v těchto organelách exprimují proapoptotické proteiny, které zase poškozují funkci mitochondrií a zabraňují produkci energie.
Kromě toho toto poškození způsobuje uvolňování proteinu z mitochondrií - cytochromu, což přispívá ke zvýšení koncentrace iontů vápníku v buňce. Zvyšování množství tohoto iontu je spouštěčem apoptózy.
Průběh apoptózy
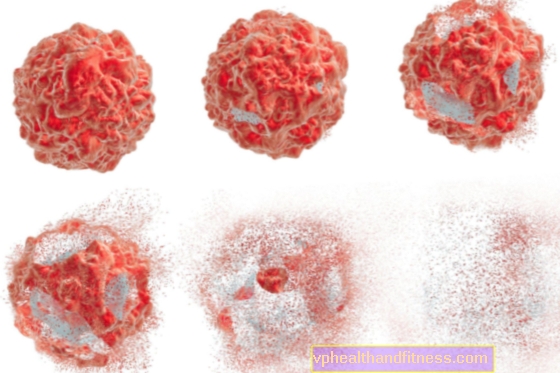
Přechod buňky na apoptózu lze poznat pozorováním jejího oddělení od ostatních, jedná se o první krok v tomto procesu. Je výsledkem posunů elektrolytů, dehydratace buněk a změn jejich tvaru. Poté je buněčné jádro fragmentováno a jsou vytvořena takzvaná apoptorická těla, jedná se o buněčné zbytky, které budou absorbovány sousedními buňkami nebo „sežrány“ makrofágy. Takový průběh apoptózy způsobuje, že je buňka „tiše“ odstraněna, a nezpůsobuje vývoj obecné reakce - zánětu.
Jak již bylo zmíněno, do tohoto procesu jsou zapojeny různé enzymy: kaspázy štěpící proteiny obsažené v jádru a cytoplazmě, transglutaminázy a endonukleolytické enzymy odpovědné za štěpení DNA. Průběh celého procesu ničení (provádění apoptózy) lze rozdělit do několika fází:
1. Fáze kontroly a rozhodování - spočívá v přenosu informací do jádra buňky o aktivaci opravných mechanismů nebo jejich opuštění a zahájení procesu rozpadu buňky. Na tomto procesu se podílejí kaspázy, proteiny BID a BAX a T lymfocyty uvolňují uvnitř buněk granzymy, které mimo jiné uvolňují ionty vápníku stimulující apoptózu.
2. Výkonná fáze - v této fázi kaspázy rozvíjejí svoji plnou funkci - ničí buněčné bílkoviny - strukturní a enzymatické:
- DNA polymeráza a DNA kináza, zabraňující opravě nukleových kyselin
- lamináty, které poškozují jadernou membránu.
V této fázi dochází k dehydrataci buňky, dalším změnám tvaru a velikosti, fragmentaci DNA (endonukleázou), fragmentaci buněk a tvorbě apoptotických těl. Tyto kaspázy jsou intracelulární enzymy, které štěpí proteiny na konkrétních místech - v dané sekvenci aminokyselin. K jejich aktivaci dochází lavinovým způsobem - aktivovaná kaspáza aktivuje další.
Je zajímavé, že navzdory rozpadu mnoha buněčných proteinů zůstávají buněčné organely nepoškozené a vstupují úplně do apoptorických těl.
3. Fáze čištění je založena na fagocytóze, tj. Absorpci buněčných zbytků, nejčastěji fantomovými buňkami - makrofágy.
Kontrola apoptózy
Apoptóza je přísně regulovaný proces - jak jeho zahájení, tak jeho průběh. Kontrolou je primárně rodina proteinů Bcl-2, zahrnují antiapoptotické proteiny - působí proti rozvoji apoptózy (např.Bcl-2, Bcl-XL, Bcl-w) a proapoptotické - podporují její výskyt poškozením mitochondriální membrány (Bid, Bak, Špatný).
Exprese nebo aktivita těchto proteinů závisí na podmínkách, ve kterých je buňka přítomna, a také na jejím stavu - pokud je poškození velké nebo vnější podmínky nejsou příznivé, aktivují se proapoptotické proteiny.
Za normálních podmínek dominují antiapoptotické proteiny a inhibují proces programované buněčné smrti. Kromě toho bylo prokázáno, že apoptóza je také řízena geny, z nichž jeden je gen p53, který patří k pro-apoptotickým faktorům. Jeho produkt, protein p53, spouští proces sebevražedné buněčné smrti, pokud je poškození genetického materiálu tak závažné, že oprava DNA není možná.
Proto je tento protein někdy označován jako „strážce genomu“, protože určuje, zda buňka zastaví buněčné dělení, aby napravila vzniklé poškození, nebo zda bude apoptóza.
Apoptóza a nemoci
Bylo prokázáno, že nerovnováha mezi tvorbou nových buněk a eliminací starých buněk je příčinou mnoha nemocí, proto je buněčná kontrola apoptózy nesmírně důležitá a její narušení může mít velmi závažné důsledky.
Pokud jsou buňky rezistentní na smrt apoptózou, může se vyvinout rakovina nebo autoimunitní onemocnění (např. Revmatoidní artritida). V obou těchto případech nemocné buňky nepodléhají apoptotickému procesu, jsou vůči němu „rezistentní“ v důsledku genetických mutací nebo abnormální aktivity pro a anti-apoptotických proteinů. Na druhou stranu, nadměrné dodržování předpisů a vylučování příliš mnoha buněk může vést k degenerativním onemocněním a poškození orgánů.
V současné době testované nejnovější onkologické léky působí ve stádiu apoptózy - mechanismem účinku je podpora přítomnosti pro-apoptotických proteinů - podpora výskytu apoptózy v nádorových buňkách. Radiační terapie a „standardní“ chemoterapie fungují podobně jako indukce apoptózy. Obě tyto léčby způsobují buněčný stres, který vede ke smrti nádorových buněk. Bohužel taková terapie není vždy účinná, protože aktivita faktorů inhibujících apoptózu se v nádorových buňkách nezřídka zvyšuje, což nejen brání boji proti nim, ale také vede k nekontrolovanému růstu a množení.
Přečtěte si také: Vývoj rakoviny nebo jak vzniká rakovina
Doporučený článek:
Vývoj nádoru - Jak se rakovina formuje o autorovi