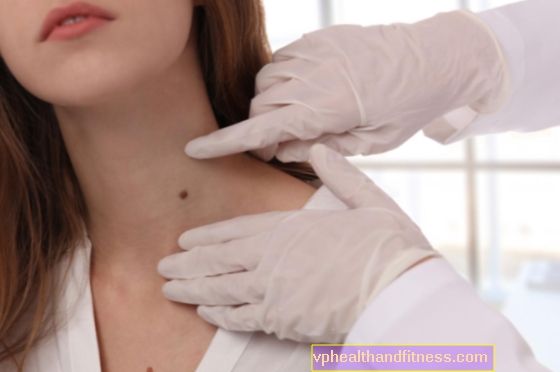
1 injekční lahvička obsahuje 5 mg nebo 35 mg agalsidázy beta.
| název | Obsah balení | Léčivá látka | Cena 100% | Naposledy změněno |
| Fabrazyme | 10 lahviček, prášek pro přípravu konečné řešení do inf. | Agalsidáza beta | 2019-04-05 |
Akce
Agalsidáza beta - rekombinantní forma lidské α-galaktosidázy A, produkovaná technologií rekombinantní DNA za použití buněčné kultury vaječníků čínského křečka (aminokyselinová sekvence rekombinantní formy a nukleotidová sekvence, která ji kóduje, jsou identické s přirozenou formou α-galaktosidázy). Je to enzym, který katalyzuje hydrolýzu GL-3. Nedostatek jeho aktivity v průběhu Fabryho choroby způsobuje ukládání GL-3 v mnoha typech buněk, včetně endotelových a parenchymálních buněk. Ošetření přípravkem vede k významnému snížení usazenin GL-3 v ledvinách, srdci a kůži. Po intravenózním podání je agalsidáza beta rychle odstraněna z oběhu a absorbována lysozomy endotelových buněk krevních cév a parenchymálních buněk. T0,5 ve eliminační fázi je 45-100 min.
Dávkování
Intravenózně. Léčba by měla být prováděna lékařem, který má zkušenosti s léčbou pacientů s Fabryho chorobou nebo jinými dědičnými metabolickými chorobami. Doporučená dávka je 1 mg / kg tělesné hmotnosti. jednou za 2 týdny U některých pacientů po počáteční dávce 1 mg / kg. každé 2 týdny po dobu 6 měsíců dávka 0,3 mg / kg používané každé 2 týdny může podporovat snížení depozit GL-3 v určitých typech buněk; dlouhodobý klinický význam těchto pozorování však nebyl stanoven. Zvláštní skupiny pacientů. U pacientů s renální nedostatečností není nutná žádná úprava dávky. Studie nebyly provedeny u pacientů s jaterní nedostatečností. Bezpečnost a účinnost nebyla stanovena u pacientů> 65 let; v současné době nelze doporučit žádný dávkovací režim. Studie u dětí ve věku 0-7 let nebyly provedeny a bezpečnost a účinnost léku v této věkové skupině nebyla stanovena; nelze doporučit žádný dávkovací režim. U dětí ve věku 8 až 16 let není nutná žádná úprava dávky. Způsob dávání. Prášek pro koncentrát pro infuzní roztok musí být rekonstituován vodou na injekci, poté zředěn 0,9% roztokem chloridu sodného intravenózně a podán jako intravenózní infuze. Počáteční rychlost infuze by neměla překročit 0,25 mg / min (15 mg / h). Pokud pacient lék dobře snáší, lze rychlost infuze postupně zvyšovat pomocí následujících infuzí. Domácí infuze mohou být zváženy u pacientů, kteří je dobře snášejí. Pacienti, u nichž se během domácích infuzí vyskytnou nežádoucí účinky, musí infuzi okamžitě zastavit a vyhledat lékařskou pomoc. Provádění následujících infuzí může vyžadovat klinické stavy. Dávka a rychlost infuze doma by měly být konstantní a neměly by být měněny bez dohledu zdravotnického pracovníka.
Indikace
Dlouhodobá substituční léčba enzymy u pacientů s potvrzenou diagnózou Fabryho choroby (nedostatek α-galaktosidázy A). Lék je indikován u dospělých, dospívajících a dětí ve věku ≥ 8 let.
Kontraindikace
Život ohrožující přecitlivělost (anafylaktická reakce) na léčivou látku nebo na kteroukoli pomocnou látku.
Opatření
Agalsidáza beta (r-hαGAL) je rekombinantní protein, proto lze u pacientů s malou nebo žádnou reziduální aktivitou enzymu očekávat vývoj IgG protilátek; IgG protilátky proti r-hαGAL se obvykle vyvinou u většiny pacientů do 3 měsíců od prvního podání přípravku. U pacientů s protilátkami proti r-hαGAL je zvýšené riziko reakcí souvisejících s infuzí a u těchto pacientů je nutná opatrnost při opětovném podávání agalsidázy beta; hladiny protilátek by měly být sledovány. U mírných až středně závažných reakcí souvisejících s infuzí může být rychlost podávání léku snížena na 10 mg / ha / nebo premedikována antihistaminiky, paracetamolem, ibuprofenem a / nebo kortikosteroidy. Stejně jako u jiných intravenózních léčivých přípravků obsahujících bílkoviny se mohou objevit hypersenzitivní reakce alergického typu; v případě závažných alergických nebo anafylaktických reakcí by mělo být podávání přípravku okamžitě přerušeno a měla by být zahájena vhodná léčba. U pacientů s pokročilým onemocněním ledvin může být renální účinek léčby agalsidázou beta omezený.
Nežádoucí aktivita
Velmi časté: bolest hlavy, parestézie, nevolnost, zvracení, zimnice, horečka, pocit chladu. Časté: nazofaryngitida, závratě, somnolence, hypoestézie, pocit pálení, letargie, synkopa, zvýšené slzení, tinnitus, periferní závratě, tachykardie, palpitace, bradykardie, návaly, hypertenze, bledost , hypotenze, návaly horka, dušnost, ucpaný nos, svírání hrdla, sípání, kašel, zhoršení dušnosti, bolesti břicha, bolesti v horní části břicha, diskomfort v horní části břicha, žaludeční diskomfort, orální hypoestézie, průjem, svědění, kopřivka, vyrážka, erytém, generalizované svědění, angioneurotický edém, otok obličeje, makulopapulární vyrážka, bolest končetin, bolesti svalů, bolesti zad, svalové křeče, bolesti kloubů, svalové napětí, muskuloskeletální ztuhlost, únava, diskomfort na hrudi, pocit horka , únava, otoky končetin, bolest na hrudi, astenie, bolest, otok obličeje, hypertermie. Méně časté: rýma, hyperestézie, třes, svědění očí, oční hyperemie, otoky uší, bolesti uší, sinusová bradykardie, periferní chlad, bronchospazmus, faryngolaryngeální bolest, rýma, rychlé dýchání, překrvení horních cest Poruchy dýchacích cest, dyspepsie, dysfagie, mramorování cyanózy, erytematózní vyrážka, svědění vyrážky, změna barvy kůže, diskomfort kůže, muskuloskeletální bolest, pocit horka a chladu, příznaky podobné chřipce, bolest v místě infuze, reakce v místě infuze, trombóza v místě vpichu, malátnost, otoky. Není známo: anafylaktoidní reakce, hypoxie, leukocytoklastická vaskulitida, snížené okysličení. Většinu nežádoucích účinků souvisejících s léčivem lze připsat tvorbě IgG protilátek a / nebo aktivaci komplementu. IgE protilátky byly detekovány u malého počtu pacientů. Bezpečnostní profil léku u dětí (> 7 let) a dospívajících se neliší od bezpečnostního profilu pozorovaného u dospělých.
Těhotenství a kojení
Nemělo by se používat během těhotenství, pokud to není nezbytně nutné (nejsou k dispozici dostatečné údaje o použití léku u těhotných žen). Agalsidáza beta může přecházet do mateřského mléka. Vzhledem k tomu, že nejsou k dispozici žádné údaje o účincích na kojence, je třeba během léčby přípravkem přerušit krmení.
Komentáře
V den podání se mohou objevit závratě, ospalost a mdloby, které mohou omezit schopnost řídit nebo obsluhovat stroje. Uchovávejte lék při teplotě 2-8 stupňů C.
Interakce
Lék by neměl být podáván s chlorochinem, amiodaronem, monobenzonem nebo gentamicinem kvůli riziku inhibice intracelulární aktivity α-galaktosidázy. Vzhledem k metabolismu agalsidázy beta se nezdá, že by byl zapojen do lékových interakcí zprostředkovaných cytochromem P450.
Přípravek obsahuje látku: Agalsidáza beta
Úhrada léku: NE




















.jpg)