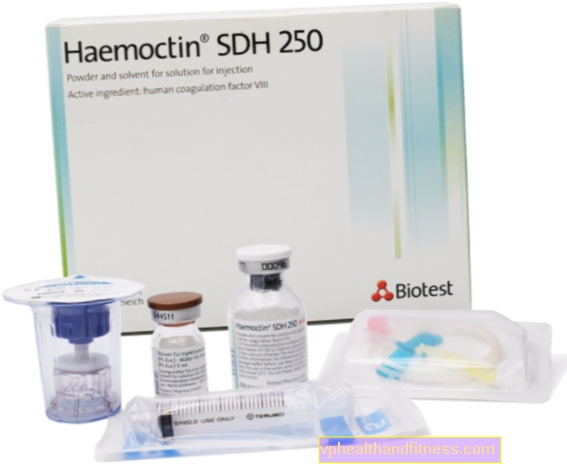
1 injekční lahvička nominálně obsahuje 250 IU, 500 IU nebo 1 000 IU koagulační faktor VIII produkovaný z lidské plazmy. Specifická aktivita přípravku je přibližně 100 IU / mg proteinu.1 injekční lahvička obsahuje až 32,2 mg sodíku (1,4 mmol).
| název | Obsah balení | Léčivá látka | Cena 100% | Naposledy změněno |
| Hemoktin | 1 lahvička + 1 lahvička pro rekonstituci, prášek a rekonstituci pro přípravu řešení kvůli šoku | Faktor VIII | 2019-04-05 |
Akce
Když se faktor VIII podává pacientovi s hemofilií, váže se na von Willebrandův faktor v pacientově oběhu. Aktivovaná část VIII urychluje transformaci součásti. X k aktivované části. X. Aktivovaná část. X převádí protrombin na trombin, který přeměňuje fibrinogen na fibrin, což umožňuje tvorbu sraženiny. Po intravenózním podání je aktivita VIII v plazmě klesá v bifázickém exponenciálním rozpadu. V počáteční fázi probíhá distribuce mezi intravaskulárním kompartmentem a dalšími kompartmenty (tělesnými tekutinami) s plazmatickým eliminačním poločasem 1-8 h. V další fázi se eliminační poločas pohybuje v rozmezí 5-18 h, s průměrnou dobou přibližně 12 h. Část úrovně aktivity VIII po intravenózním podání 1 IU část VIII na kg živé hmotnosti je asi 2%. Průměrná doba přítomnosti léčiva v těle je přibližně 15 hodin, clearance je přibližně 155 ml / h.
Dávkování
Podávání by mělo být zahájeno pod dohledem lékaře se zkušenostmi s léčbou hemofilie. Část aktivity. VIII v plazmě je vyjádřen buď v procentech (ve srovnání s normální lidskou plazmou), nebo v IU. (s odkazem na mezinárodní standardní část VIII v plazmě). Část mezinárodní jednotky (IU) VIII odpovídá množství dílů VIII obsažený v 1 ml normální lidské plazmy. Výpočet požadované dávky VIII byl založen na empirickém pozorování, že 1 IU část VIII na 1 kg tělesné hmotnosti zvyšuje aktivitu části VIII v plazmě od 1 do 2% normální aktivity. Substituční léčba. Potřebná část dávky. VIII se stanoví pomocí následujícího vzorce: požadovaná dávka (IU) = tělesná hmotnost (kg) x požadovaný přírůstek faktoru VIII (% normální) x 0,5. Dávka, frekvence a trvání substituční léčby musí být individuálně upraveny podle potřeb pacienta (v závislosti na stupni deficitu části VIII, na místě a rozsahu krvácení a na klinickém stavu pacienta). Níže jsou uvedena doporučení pro jednotlivé minimální úrovně dílu. VIII v krvi pro různé typy krvácení. Je nutné časné krvácení do kloubů, svalů nebo z úst VIII je 20-40%: opakujte infuzi každých 12-24 hodin po dobu alespoň 1 dne, dokud není krvácení zastaveno, jak je naznačeno úlevou od bolesti nebo uzdravením. Rozsáhlejší krvácení do kloubů, svalů nebo hematomu - požadovaná hladina VIII je 30-60%: opakujte infuzi každých 12-24 hodin po dobu 3-4 dnů nebo déle, dokud bolest a kondice nevymizí. Život ohrožující krvácení - požadovaná úroveň VIII je 60-100%: opakujte infuzi každých 8-24 hodin, dokud není hrozba odstraněna. Malé chirurgické zákroky, včetně extrakce zubů - část vyžadující úroveň VIII je 30-60%: opakujte infuzi každých 24 hodin, po dobu nejméně 1 dne, dokud se nezhojí. Hlavní chirurgické zákroky - požadovaná úroveň VIII je 80-100% v pre- a pooperačním období: opakujte infuzi každých 8-24 hodin, dokud se rána dostatečně nezhojí, poté pokračujte v léčbě po dobu nejméně 7 po sobě jdoucích dní, abyste udrželi aktivitu VIII do 30-60%. Množství, které má být podáno, a frekvence podávání by měly být vždy upraveny podle klinické účinnosti v konkrétním případě. Během léčby se doporučuje odpovídající stanovení hladin částic. VIII k určení dávky a frekvence opakovaných infuzí. Zejména při velkých chirurgických zákrocích je nutné pečlivě sledovat substituční léčbu pomocí koagulačních testů (část VIII s plazmatickou aktivitou). Prevence. Pro dlouhodobou profylaxi krvácení u pacientů s těžkou hemofilií jsou obvyklé dávky 20-40 IU / kg. v intervalech 2 až 3 dnů. V některých případech, zejména u mladších pacientů, mohou být nutné kratší intervaly dávek nebo vyšší dávky. Pacienti s inhibitory. U pacientů léčených přípravkem je třeba sledovat vývoj inhibitorů částic. VIII. U pacientů s vysokou hladinou inhibitoru je léčba částí VIII může být neúčinný a je třeba zvážit další terapeutické možnosti. Léčba těchto pacientů by měla být pod dohledem lékaře, který má zkušenosti s péčí o pacienty s hemofilií.Lék by měl být podáván intravenózně rychlostí 2-3 ml / min. K přípravě a podávání léku používejte pouze rozpouštědla a složky poskytované výrobcem a postupujte podle pokynů výrobce.
Indikace
Léčba a profylaxe krvácení u pacientů s hemofilií A (vrozený nedostatek faktoru VIII). Přípravek neobsahuje Von Willebrandův faktor ve farmakologicky účinném množství, a proto není indikován u von Willebrandovy choroby.
Kontraindikace
Přecitlivělost na léčivou látku nebo na kteroukoli pomocnou látku.
Opatření
Sledujte vývoj anti-neutralizujících protilátek. VIII (inhibitory) prostřednictvím příslušných klinických pozorování a laboratorních testů. Riziko vývoje inhibitorů závisí na expozičním období VIII, přičemž riziko je nejvyšší během prvních 20 dnů expozice. Vzácně se inhibitory mohou vyvinout po prvních 100 dnech expozice. U pacientů s existujícími rizikovými faktory pro kardiovaskulární onemocnění může substituční léčba faktorem VIII zvýšit kardiovaskulární riziko. Pokud je vyžadováno zařízení pro centrální venózní přístup (CVAD), mělo by být zváženo riziko komplikací souvisejících s CVAD, včetně lokálních infekcí, bakteremie a trombózy v místě katétru. Přes použití metod inaktivace infekčních agens nelze zcela vyloučit přenos známých a neznámých patogenů přípravkem. Opatření přijatá k prevenci infekcí jsou považována za účinná proti obaleným virům, jako jsou HIV, HBV a HCV a neobalenému viru hepatitidy A (HAV); mohou mít omezenou hodnotu proti neobaleným virům, jako je parvovirus B19. Infekce parvovirem B19 může být nebezpečná pro těhotné ženy (infekce plodu) a pro lidi s imunodeficiencí nebo zvýšenou erytropoézou (např. Hemolytická anémie). U pacientů, kteří jsou pravidelně nebo opakovaně léčeni léky z lidské plazmy, se doporučuje odpovídající očkování (proti hepatitidě A a B). Pokud dojde k alergické nebo anafylaktické reakci, podávání léku by mělo být přerušeno; v případě šoku by měla být zahájena vhodná léčba. U pacientů na dietě s nízkým obsahem sodíku je třeba vzít v úvahu obsah sodíku v přípravku.
Nežádoucí aktivita
Velmi časté (u dosud neléčených pacientů): inhibice faktoru VII. Méně časté (u pacientů již léčených): inhibice faktoru VII. Vzácné: horečka, přecitlivělost nebo alergické reakce (včetně: angioedému, pocitu pálení a píchání v místě infuze, zimnice, návalů, generalizované kopřivky, bolesti hlavy, vyrážky, hypotenze, somnolence, nevolnosti, neklidu, tachykardie, pocitu tlaku hrudník, brnění, zvracení, sípání), které v některých případech mohou vést k závažné anafylaxi (včetně šoku). Velmi vzácné: vyrážka, kopřivka, erytém.
Těhotenství a kojení
Neexistují žádné reprodukční studie na zvířatech. S používáním přípravku u těhotných a kojících žen nejsou žádné zkušenosti - používejte pouze v nezbytně nutných případech.
Komentáře
Důrazně se doporučuje, aby se při každém podání přípravku zaznamenal název a číslo šarže, aby bylo možné pacienta spojit s šarží přípravku.
Přípravek obsahuje látku: Faktor VIII
Úhrada léku: NE